国际水准!先声东元塞来昔布胶囊ANDA申请获美国FDA批准
发布日期:2020-05-19 浏览次数:
喜讯!
收到美国食品药品监督管理局(FDA)通知
其向美国FDA申报的
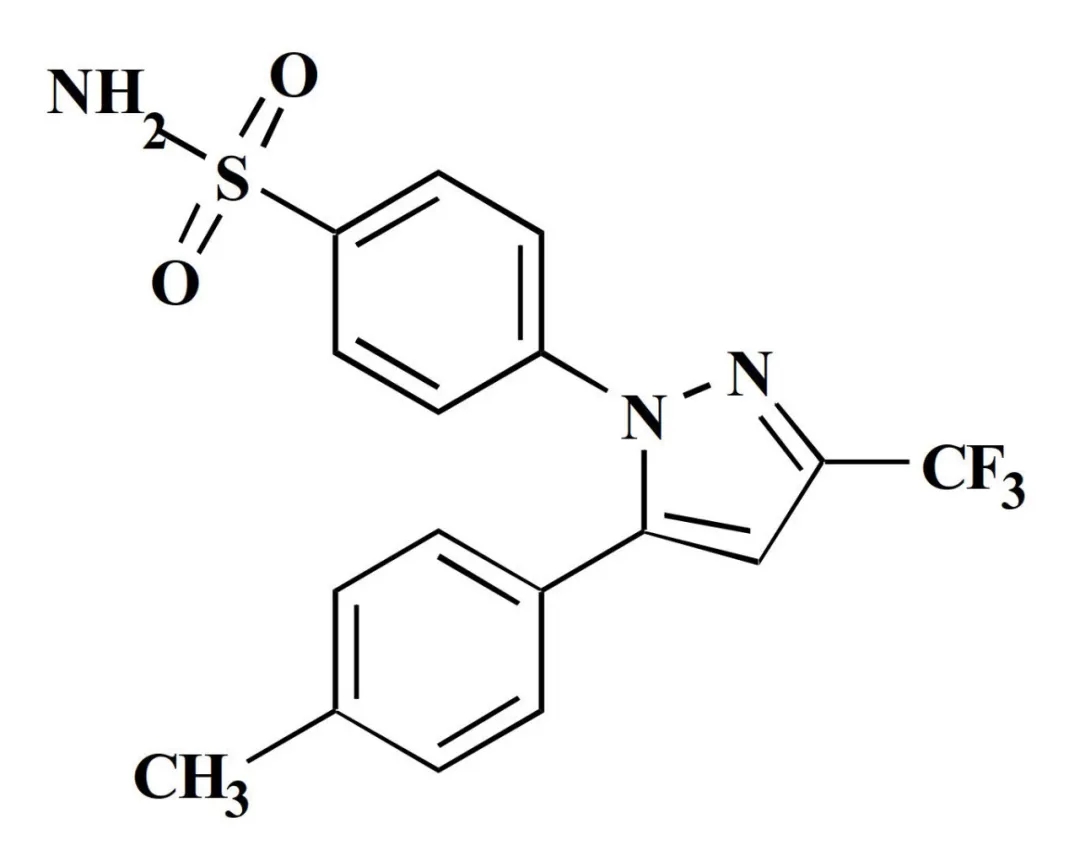
塞来昔布胶囊简略新药申请(ANDA)已经获得批准!

据了解,塞来昔布胶囊是先声药业的第一个中美双报产品,目前国内申报也已完成,审评正在进行中。
塞来昔布胶囊项目于2019年7月31日递交ANDA申报材料,审评过程仅用时9个月13天。2020年1月13日-17日,先声东元接受了FDA对于塞来昔布胶囊的药品批准前现场检查(PAI),并以零缺陷顺利通过cGMP,这表明先声东元药品生产和质量控制的全过程达到了国际水平。公司表示后期将尽快启动美国市场的商业化销售和其它国际市场的注册工作,以惠及更多患者。
塞来昔布是一种非甾体类抗炎药,通过抑制环氧化酶-2 (COX-2)来抑制前列腺素生成,具有抗炎镇痛的疗效。获FDA批准用于治疗骨关节炎(OA)、类风湿关节炎(RA)、两岁及以上患者的幼年型类风湿关节炎(JRA)、强制性脊柱炎(AS)、急性疼痛(AP)以及原发性痛经(PD)。
塞来昔布胶囊原研药持证商为G.D. Searle LLC(现隶属于Pfizer Inc),1998年在美国获批上市,商品名为CELEBREX®,该产品于2000年在中国获得进口药品上市批准,商品名为西乐葆®。
塞来昔布胶囊2018年和2019年在全球销售额分别为10.692亿美元、11.213亿美元;2018年和2019年在美国地区销售额分别为1.835亿美元、2.122亿美元(数据来源于Newport数据库)。
素材来源:先声药业