一、政策简讯
No.1 5月18日,国家药监局药审中心发布关于药品专利纠纷早期解决机制相关专利信息登记平台公开测试等有关事宜的通知。测试期间已按要求登记的相关专利信息经药品上市许可持有人确认后公开,作为化学仿制药、中药同名同方药以及生物类似药申请人作出专利声明的依据信息,测试时间至5月31日。
No.2 5月20日,国家药监局综合司公开征求《医疗器械临床评价技术指导原则(征求意见稿)》等文件意见。本次指导原则征求意见稿包括以下7个文件:1)医疗器械临床评价技术指导原则(征求意见稿);2)体外诊断试剂临床试验指导原则(征求意见稿);3)医疗器械等同性论证技术指导原则(征求意见稿);4)决策是否开展医疗器械临床试验技术指导原则(征求意见稿);5)医疗器械注册申报临床评价报告技术指导原则(征求意见稿);6)免于进行临床试验的体外诊断试剂方法学比对技术指导原则(征求意见稿);7)免于进行临床评价医疗器械目录(征求意见稿)。反馈意见截止时间为2021年5月31日。
二、药企动态
No.1 2021年5月16日迈瑞发布公告称,为进一步加强化学发光产品及原料的核心研发能力建设,优化上下游产业链的全球化布局,拟通过全资子公司以现金约42亿人民币(5.45亿欧元)收购IVD原材料公司瑞典Hytest Invest Oy公司(海肽生物)的100%股权。
No.2 5月17日,深圳亚辉龙生物科技股份有限公司(以下简称:亚辉龙)正式在科创板挂牌上市,股票代码为688575。发行价为14.80元/股,开盘价为65.00元,较发行价暴涨339.19%。收盘报65.00元,市值超259.20亿元。截至2021年1月31日,公司自主研发生产的体外诊断产品已经取得一类医疗器械产品备案凭证21项、二类医疗器械产品注册证154项、三类医疗器械产品注册证55项;已经取得欧盟CE认证的产品达263项,包括List B类20项、Others类241项、I类2项。
No.3 5月17日,睿昂基因正式在科创板挂牌上市,股票代码为688217。发行价为18.42元/股,开盘价为95.00元,较发行价暴涨415.74%。收盘报106.42元,市值59.15亿。睿昂基因成立于2012年,是一家拥有自主品牌分子诊断产品的生命科学企业,主营业务为体外诊断产品的研发、生产、销售及科研、检测服务。其主要产品为分子诊断试剂,主要应用于检测患者疾病相关基因状态,为疾病诊断、风险评估、疾病分型、靶向药物选择和疗效监测等个性化治疗方案的制定提供分子水平的检测依据。目前公司已经与全国超过150家三级甲等医院保持着稳定的合作关系,产品及科研、检测服务覆盖全国。
No.4 2020年12月29日,苏州瑞博生物技术有限公司申请科创板IPO获上交所受理,国泰君安担任公司保荐机构。2021年5月21日,上交所发布文件《根据《上海证券交易所科创板股票发行上市审核规则》第六十七条的有关规定,本所决定终止对你公司首次公开发行股票并在科创板上市的审核。公开资料显示,瑞博生物成立于2007年,是一家专注于小核酸药物的研究、开发和生产的创新药企。截至招股说明书签署日,瑞博生物开展了十余款产品的研究,主要围绕糖尿病、肿瘤、眼科疾病、乙肝、高血脂等疾病领域开展。
No.5 4月30日,上交所发布关于终止上海奥普生物医药股份有限公司首次公开发行股票并在科创板上市审核的决定。2021年4月23日,奥普生物和其保荐人中信证券股份有限公司申请撤回申请文件。根据有关规定,上交所决定终止对奥普生物首次公开发行股票并在科创板上市的审核,奥普上市梦碎。奥普生物是国内体外诊断产品较早的供应商之一,专注于POCT检测仪器、POCT诊断试剂的研发、生产和销售,是一家研发驱动型高新技术企业。
三、药品审批
No.1 5月18日,信达生物宣布美国食品药品监督管理局(FDA)正式受理了其和美国礼来制药公司联合开发的创新药物PD-1单克隆抗体达伯舒联合培美曲塞和铂类用于非鳞状非小细胞肺癌(NSCLC)一线治疗的新药上市申请 (BLA),这标志着中国自主研发的创新生物药的完整上市申请首次被美国FDA受理并进入正式审评阶段,达伯舒(通用名:信迪利单抗注射液,sintilimab)也成为第一个完整上市申请被欧美国家监管机构受理并进入正式审评阶段的中国自主研发的创新生物药。
No.2 5月18日,开拓药业发布公告,美国食品和药物管理局(FDA)已同意普克鲁胺用于治疗住院新冠(COVID-19)患者的III期临床试验,该试验将同时招募男女性患者。这是开拓药业继普克鲁胺用于治疗轻中症COVID-19患者的III期临床试验之后第2个获得FDA同意的关键性全球多中心III期临床试验。同时,FDA亦已同意在轻中症COVID-19 III期临床试验中拓展纳入女性患者。
No.3 5月20日,阿诺医药宣布已向美国食品药品监督管理局(FDA)递交了其原创新药口服PD-L1抑制剂AN4005的临床试验申请(IND)。阿诺医药将开展此药物安全性和药代动力学评估的临床一期试验,患者入组也将于美国启动。
No.4 5月21日,FDA加速批准强生公司EGFR/c-Met双抗Rybrevant (amivantamab-vmjw) 上市,用于治疗铂类化疗后进展的EGFR外显子20插入突变的转移性非小细胞肺癌(NSCLC)患者。这是FDA批准的首个针对该类突变的药物。
No.5 近日,健艾仕生物(GenEros BioPharma)透露,该公司的创新STAT5抑制剂clinflamozyde已获美国FDA批准进入临床试验,用于新冠疾病的治疗。在细胞和动物模型中,健艾仕生物发现clinflamozyde对细胞因子风暴有显著抑制作用,且不影响抗病毒的干扰素通路。
No.6 近日,百时美施贵宝BMS宣布,美国FDA已批准Opdivo(nivolumab)扩展适应症,作为辅助疗法,用于治疗接受完全切除手术的食管癌或胃食管连接部(GEJ)癌患者。这些患者在接受过新辅助放化疗(CRT)后发现残余病理学疾病。新闻稿指出,Opdivo是首款获批辅助治疗这一患者群的免疫疗法。
No.7 近日,美国FDA宣布,批准强生旗下杨森(Janssen)公司开发的EGFR/MET双特异性抗体疗法Rybrevant(amivantamab-vmjw)上市,用于治疗携带EGFR外显子20插入突变的非小细胞肺癌患者(NSCLC)。新闻稿指出,这是FDA批准用于治疗这一患者群的首款精准疗法。该双特异性抗体疗法已经被中国国家药监局(NMPA)纳入突破性治疗品种,目前在中国展开多项临床试验,其中包括与第三代EGFR酪氨酸激酶抑制剂lazertinib联用,一线治疗携带EGFR突变的局部晚期或转移性非小细胞肺癌。
Amivantamab可以通过多种机制杀伤NSCLC细胞
No.8 5月21日,武田(Takeda)公司宣布,美国FDA已受理口服蛋白激酶抑制剂maribavir(TAK-620)的新药申请(NDA)。Maribavir是武田最近6个月内接受美国FDA监管审评的第4个新分子实体。新闻稿指出,如果获批,maribavir将成为首个治疗接受器官移植或造血细胞移植后,发生难治性、有或无耐药性(R/R)巨细胞病毒(CMV)感染患者的药物。
No.9 5月21日,葛兰素史克(GlaxoSmithKline)和Vir Biotechnology宣布,欧洲药品管理局(EMA)人用药品委员会(CHMP)对COVID-19中和抗体疗法sotrovimab发表积极意见,支持其获批用于治疗不需要补充氧气,但有发展为严重COVID-19潜在风险的成人和青少年患者。
No.10 近日,金斯瑞发布公告,欧盟EMA已经正式受理了其控股公司传奇生物cilta-cel上市申请。cilta-cel是传奇生物自主研发的靶向B细胞成熟抗原(BCMA)的定向嵌合抗原受体T细胞(CAR-T)疗法。 该款药物已经先后获得了FDA授予的突破性疗法认定、EMA授予的优先药物资格,同时也是中国首个获得突破性疗法资格的药物。2017年12月,杨森(强生旗下公司)与传奇生物达成一项许可协议,获得了在全球共同开发和推广cilta-cel的权利。
No.11 5月17日,CDE官网显示上海璎黎药业自主研发的创新药PI3Kδ选择性抑制剂林普利司片(代号:YY-20394)上市申请已获得国家药监局受理,用于治疗复发/难治滤泡性淋巴瘤。林普利司是璎黎药业自主研发的1类创新药,今年2月8日,恒瑞医药与璎黎药业签订战略合作协议,恒瑞医药将对璎黎药业进行2000万美金股权投资,璎黎药业授予恒瑞针对林普利司在大中华地区的联合开发权益以及排他性独家商业化权益。
No.12 5月18日,CDE官网显示浙江医药注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)获CDE拟突破性疗法认定并开始公示,拟用于HER2阳性晚期乳腺癌二线治疗。
No.13 5月18日,康方生物发布公告,其研发的CD47单抗(AK117)获NMPA批准开展治疗中高危骨髓增生异常综合症(MDS)的I/II期临床研究。CD47-SIRPα是吞噬细胞的抑制途径,但CD47同时广泛表达在肿瘤细胞中,阻断该通路可以开启吞噬肿瘤细胞的免疫机制,因此该机制一度被认为是一个大有希望的新靶点。
No.14 5月18日,诺诚健华宣布收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,公司自主研发的新型酪氨酸激酶2(Tyrosine Kinase 2, TYK2)抑制剂ICP-332已获批开展临床试验,这也是诺诚健华第五款进入临床阶段的创新药。
TYK2抑制剂临床研究进展
No.15 5月18日CDE官网显示,默沙东MK-1026片临床申请获国家药监局受理。是国内第3款申报临床的BTK-C481S抑制剂。
No.16 5月19日,CDE官网显示Epizyme公司Tazemetostat(他折司他)临床申请已获国家药监局受理,是国内第3家申报临床的EZH2抑制剂。
No.17 5月20日,CDE官网显示,拜耳larotrectinib(拉罗替尼)胶囊和口服液上市申请已获得国家药监局受理。根据此前在国内登记的临床试验,预计申报上市的适应症为:治疗携带NTRK融合基因的局部晚期或转移性实体瘤成人和儿童患者。
四、投融资
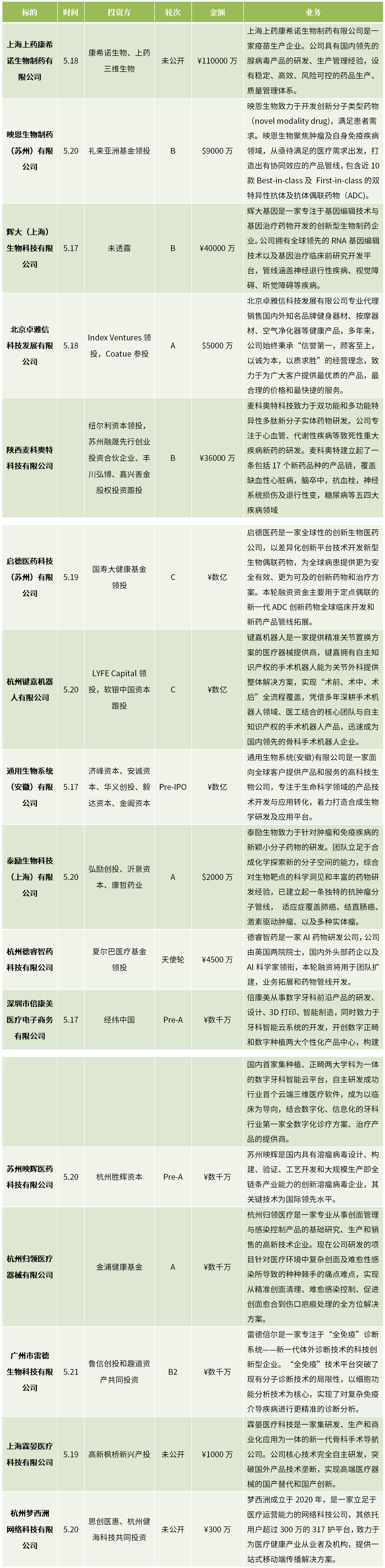
五、医药科技
No.1 5月20日,清华大学免疫研究所徐萌团队联合中科院北京基因组研究所韩大力团队,在 《Cancer Cell》发表了题为:The loss of RNA N6-adenosine methyltransferase Mettl14 in tumor-associated macrophages promotes CD8+ T cell dysfunction and tumor growth 的研究论文。该研究揭示了特定肿瘤相关巨噬细胞亚群通过表观转录组层面调控CD8+ T细胞功能的新机制:m6A甲基化酶METTL14在C1q+ 巨噬细胞中的丧失,导致巨噬细胞中Ebi3转录本上m6A修饰的降低和EBI3表达量的增加,进而诱导肿瘤浸润的CD8+ T细胞的功能失调。
文章配图(来源:cancer cell)
No.2 近日,美国德州大学MD安德森癌症中心的 Nicholas Navin 团队等在《Nature》发表了题为:Breast tumours maintain a reservoir of subclonal diversity during expansion 的研究论文。在这项研究中,研究团队开发了一种新的单细胞DNA测序方法:声学细胞标记法(ACT)。通过对乳腺癌组织和肿瘤细胞系进行ACT测序,发现它们由大量的亚克隆组成,而在原发性肿瘤进展过程中存在一段短暂的基因组不稳定期,随后是持续的拷贝数进化,肿瘤细胞重新分化了基因组,并且没有保留等基因特性,表明三阴性乳腺癌在原发性肿瘤生长过程中持续染色体畸变并维持亚克隆多样性。
ACT方法与技术性能(来源:nature)
No.3 5月14日,浙江大学转化医学研究院吕志民教授团队和中国海洋大学于日磊教授团队合作,在《Molecular Cell》发表了题为:SUCLA2-coupled regulation of GLS succinylation and activity counteracts oxidative stress in tumor cells 的研究论文。该项研究发现,在胰腺导管腺癌中呈现谷氨酰胺酶(GLS)高表达,相比于正常细胞,胰腺导管腺癌细胞的生长和存活对于谷氨酰胺代谢表现出更强的依赖性。重要的是,在GLS蛋白上也发现了琥珀酰化修饰,该修饰发生在K311位点,可由琥珀酰辅酶A直接介导。琥珀酰化修饰促进了GLS由单体向有活性的四聚体的转换,从而提高了其催化活性,增强了对谷氨酰胺的分解代谢。
No.4 5月20日,礼来(Eli Lilly and Company)宣布,其葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体双重激动剂tirzepatide,在名为SURPASS-4的临床试验中达到主要终点与所有关键性次要终点。与活性对照组相比,在心血管(CV)风险增加的2型糖尿病成人患者中,三种不同剂量tirzepatide均显著降低患者的糖化血红蛋白(A1C)和体重。接受最高剂量(15 mg)的患者组,在治疗52周后,tirzepatide成功使43%患者A1C达到正常人水平,平均体重减少11.7公斤。
No.5 5月19日,百时美施贵宝(BMS)公布其2/3期RELATIVITY-047临床试验的结果。该试验表明,固定剂量抗LAG-3抗体relatlimab和抗PD-1抗体Opdivo(nivolumab)组合疗法与Opdivo单药相比,在既往未经治疗的转移性或不可切除的黑色素瘤患者中表现出具有统计学意义和临床意义的无进展生存期(PFS)获益。
No.6 5月18日, Sarepta Therapeutics展示了其在研基因疗法SRP-9001的最新临床试验结果。SRP-9001通过将编码微抗肌萎缩蛋白(micro-dystrophin)的转基因递送至肌肉组织,从而让肌肉细胞产生微抗肌萎缩蛋白,治疗杜氏肌营养不良症(DMD)。试验结果证明这种疗法能有效升高人体内抗肌萎缩蛋白的表达水平,且安全性与耐受性良好。