一、政策简讯
No.1 7月13日,国家药监局药审中心发布关于公开征求ICH指导原则《S12:基因治疗产品的生物分布研究》意见的通知。本指导原则范围内的GT产品包括通过所转导的遗传物质的转录或翻译而发挥作用的产品。GT产品的举例可包括:纯化的核酸(例如,质粒和RNA)、表达特定基因(包括编辑宿主基因组的产品)的基因修饰微生物(例如,病毒、细菌、 真菌)、离体基因修饰的人类细胞。拟在体内改变宿主基因组但无特定转录或翻译(即通过非病毒方法递送核酸酶和向导RNA)的产品也在本指导原则范围之内。虽然溶瘤病毒在某些地区目前不被视为GT,但本品指导原则所提出的基本原则仍适用于未通过基因修饰表达特定基因的溶瘤病毒产品。BD是GT产品在生物学相关动物中给药部位、靶组织和非靶组织包括体液(例如,血液、脑脊液、玻璃体液)在内的体内分布、存续和清除。GT产品通过排泄(粪便)、分泌(尿液、唾液、鼻咽液等)或通过皮肤(脓疱、疮、伤口)释放出体外称之为“脱落”。GT产品脱落特征的非临床评价在本指导原则的适用范围之外。
二、药企动态
No.1 7月15日,礼来(Eli Lilly and Company)和Banner阿尔茨海默病研究所(Banner Alzheimer's Institute)宣布达成一项战略研究合作协议,以推进礼来正在进行的3期临床试验。该随机双盲、安慰剂对照的3期临床试验TRAILBLAZER-ALZ 3将在有与阿尔茨海默病相关的认知和功能下降风险的患者中,评估礼来在研抗体疗法donanemab减缓阿尔茨海默病临床进展的可能性,无论受试者是否携带APOE4基因。试验计划在今年晚些时候开始入组。该药物最新2期临床试验达到了试验主要终点,在接受donanemab治疗患者,其阿尔茨海默病量表(iADRS)评分降低幅度比安慰剂组减少了32%(p=0.04),这意味着患者的认知和日常生活能力的衰退速度得到缓解。同时,正电子扫描(PET)成像显示,donanemab能够迅速清除患者大脑中的淀粉样蛋白沉积,在接受治疗6个月后,40%患者的PET检测呈阴性,意味着他们大脑中淀粉样蛋白沉积的水平和健康人没有显著区别。
No.2 7月12日,诺诚健华/渤健宣布两家公司就BTK抑制剂奥布替尼达成许可及合作协议。根据协议条款,渤健将拥有奥布替尼在多发性硬化领域全球独家权利,以及除中国(包括香港、澳门和台湾)以外区域内的某些自身免疫性疾病领域的独家权利,诺诚健华将保留奥布替尼在肿瘤领域的全球独家权利,以及某些自身免疫性疾病在中国(包括香港、澳门和台湾)的独家权利。诺诚健华将获得1.25亿美元首付款,未来有资格获得最多8.125亿美元的潜在临床开发里程碑和商业里程碑付款。诺诚健华还将有资格因合作约定的任何产品潜在未来净销售额获得在百分之十几范围内从低至高的分层特许权使用费。交易的完成取决于反垄断法审查,包括美国1976年的Hart-Scott-Rodino (HSR) 反垄断改进法案,以及其他完成条件惯例。
No.3 根据港交所7月15日发布的最新公示,圣诺制药Sirnaomics已递交IPO申请并获得受理,拟在主板挂牌上市。而在两周前的7月2日,圣诺制药刚刚宣布完成了 $1.05 亿美元E轮融资。据悉,圣诺制药此次IPO的独家担保人为中金公司,此次募集款项的49.6%将用于核心候选药物STP705的研发和商业化;12.7%将用于PNP -STP707的开发;13.1%将用于拨付给N-乙酰半乳糖胺计划产品,如STP122G、STP133G及STP144G;其他mRNA临床前候选药物的研发则占了13.3%。
No.4 7月15日晚间,博雅生物发布公告宣布,控股股东高特佳集团通过协议转让方式将其持有的 69,331,978 股股份(占博雅生物总股本的16%)转让给华润医药控股,并已在中国结算深圳分公司办理完成过户登记手续。博雅生物通过公告表示,在本次股份转让完成后,表决权委托随即发生法律效力,华润医药控股将持有其 69,331,978 股股票,并合计拥有其126,381,618 股股票(占其总股本的 29.17%)的表决权,为博雅生物第一大股东。
No.5 7月13日,腾盛博药在港交所上市,共发行1.11亿股股份,发行定价22.25港元,由摩根士丹利和UBS联合保荐。 腾盛博药成立于2017年,致力于促进中国及全球就重大传染病(如HBV、HIV、MDR/XDR革兰氏阴性菌感染)及其他具有重大公共卫生负担的疾病(如中枢神经系统(CNS)疾病)的疗法,其业务模式以内部药物研发与授权引进相结合为主。目前,腾盛博药已经形成针对乙肝(HBV)、艾滋病(HIV)、新冠病毒COVID-19等传染疾病和针对抑郁症等CNS疾病在内的10多条新药研发管线,涵盖临床前到临床阶段多个项目。针对HBV,腾盛博药目前正在开发其核心产品BRII-179(一种HBV特异性B细胞和T细胞治疗疫苗)及BRII-835(一种HBV靶向siRNA,属高度创新及新兴的减少HBV抗原治疗方法)。对于BRII-179,腾盛博药已在中国、香港、新西兰、澳大利亚、泰国及韩国完成1b/2a期临床研究,最终临床研究报告已于2021年5月24日发布。而BRII-835目前正在中国开展2期临床研究。
腾盛博药产品管线,图片来源:腾盛博药招股书
No.6 7月16日上午9时30分,总部位于光谷的康圣环球基因技术有限公司,通过“云敲钟”的形式与香港时间连线直播,正式登陆港交所主板挂牌上市。康圣环球证券代码9960.HK,将发售226,405,000股,募资约35%或675.9百万港元将分配至销售及营销其现有的特检服务线以涵盖更多医院,尤其是三级医院;约20%或386.2百万港元将分配至现有特检服务线的研发,以采用创新检测技术及持续扩大其检测服务组合等。经过近20年发展,公司现已在中国独立血液学临床特检行业成功确立领导地位,根据弗若斯特沙利文的资料,以收入计,康圣环球占据最大(42.3%)的市场份额,近乎达到血液学特检市场的半壁江山,占据了绝对的龙头地位。
No.7 7月13日,证监会同意南京诺唯赞生物科技股份有限公司科创板IPO注册,即将敲钟上市。公开资料显示,诺唯赞是一家围绕酶、抗原、抗体等功能性蛋白及高分子有机材料进行技术研发和产品开发的生物科技企业,依托于自主建立的关键共性,先后进入了生物试剂、体外诊断业务领域,并正在进行抗体药物的研发,是国内少数同时具有自主可控上游技术开发能力和终端产品生产能力的研发创新型企业。
三、药品审批
No.1 7月11日,开拓药业宣布福瑞他恩(KX-826)治疗雄激素性脱发的II期临床试验申请已获得美国FDA同意开展。
福瑞他恩与非那雄胺的作用机制区别
No.2 7月13日,开拓药业发出公告,称其自主研发的基于蛋白降解嵌合体(PROTAC)技术开发的新型靶向雄激素受体(AR)的GT20029,已获得FDA的临床试验许可,将开展治疗雄激素性脱发和痤疮的研究。GT20029是全球首款进入临床阶段的外用PROTAC化合物, 继2021年4月获药监局批准开展I期临床试验, 在美国也进入临床阶段。
No.3 7月14日,Alkeus宣布FDA授予ALK-001(C20-D3-维生素A)突破性疗法称号,用于治疗斯特格氏病。目前,尚无批准的斯特格氏病治疗药物。ALK-001 是唯一获得斯特格氏病突破性疗法认定的药物。
No.4 7月15日,美国FDA心血管和肾脏药物咨询委员会(CRDAC)投票反对批准珐博进/阿斯利康开发的口服HIF-PH抑制剂罗沙司他(Roxadustat)用于治疗慢性肾病贫血患者的上市申请。
No.5 7月16日,石药发出公告,宣布抗体偶联药物SYSA1801 IND申请获得FDA的批准,拟开展Claudin 18.2阳性表达晚期胰腺癌的临床试验。I期临床试验旨在评估SYSA1801的安全性、耐受性、药代动力学特性及初步疗效。SYSA1801 已于今年获美国FDA颁发针对治疗胰腺癌的孤儿药资格认定。
No.6 近日,强生(Johnson & Johnson)旗下杨森(Janssen)公司宣布,美国FDA批准Darzalex Faspro联合泊马度胺和地塞米松(Pd),用于治疗既往接受过至少一种前期治疗的多发性骨髓瘤(MM)成人患者。这一批准标志着Darzalex Faspro 治疗多发性骨髓瘤的第6个适应症。
No.7 近日,Kadmon公司宣布,美国FDA批准该公司的Rezurock(belumosudil)上市,用于治疗12岁以上的慢性移植物抗宿主病(cGVHD)患者,这些患者已经接受过两种前期全身性治疗。新闻稿指出,Rezurock是FDA批准的首款ROCK2抑制剂,ROCK2介导的信号通路在调节炎症和纤维化反应中具有重要作用。
Belumosudil作用机制图示
No.8 近日,辉瑞(Pfizer)和BioNTech联合宣布,美国FDA已经授予其为mRNA新冠疫苗递交的生物制品许可申请(BLA)优先审评资格,用于在16岁以上人群中预防COVID-19。
No.9 7月14日,德琪医药宣布已向台湾卫生福利部食品药物管理署(TFDA)提交同类首款选择性核输出抑制剂塞利尼索(selinexor)的新药上市申请,用于治疗三个适应症:与硼替佐米、地塞米松联合或与地塞米松联合治疗复发难治性多发性骨髓瘤(RRMM)患者;单药治疗既往接受过至少二线系统治疗的成人复发难治性弥漫性大B细胞淋巴瘤(rrDLBCL)患者(包括由滤泡性淋巴瘤转化的)。
No.10 7月16日,经国务院联防联控机制有关部门组织论证,国药集团中国生物北京生物制品研究所新冠病毒灭活疫苗获批在3-17岁人群中紧急使用。中国新冠灭活疫苗正式获批在该年龄段开展紧急使用。
No.11 7月12日,CDE官网公示,武田口服小分子新药mobocertinib胶囊上市申请已正式获国家药监局受理。是国内申报上市的首款用于EGFR 20号外显子(Exon20)插入突变NSCLC的疗法,同时该产品的上市申请也被CDE纳入了优先审评。
No.12 7月12日,CDE官网显示,信达生物纤维细胞生长因子受体(FGFR)1/2/3抑制剂Pemigatinib片的上市申请拟纳入优先审评,用于既往至少接受过一种系统性治疗,且经检测确认存在有FGFR2融合或重排的晚期、转移性或不可手术切除的胆管癌成人患者。
No.13 7月12日,CDE官网显示,辉瑞Lorlatinib片(劳拉替尼 )上市申请拟纳入优先审评,拟用于既往接受过一种或多种间变性淋巴瘤激酶(ALK)酪氨酸激酶抑制剂(TKI)治疗的ALK阳性局部晚期或转移性非小细胞肺癌 (NSCLC) 患者。
No.14 7月12日,CDE官网显示,强生的JNJ-56136379片、JNJ-73763989注射剂被拟纳入突破性疗法,均用于治疗慢性乙型肝炎病毒感染。
No.15 7月13号,贝达药业发出公告,称盐酸恩沙替尼胶囊上市许可申请已获得国家药监局受理,拟用于间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
No.16 7月13日,赛诺菲注射用重组人凝血因子VIII Fc-血管性血友病因子-XTEN融合蛋白(efanesoctocog alfa,rFVIIIFc-VWF-XTEN,BIVV001)获CDE拟突破性疗法,拟定的适应症是用于患有A型血友病的成人和儿童:(1)常规预防治疗,用于减少出血的发生频率;(2)出血的按需治疗;(3)围手术期出血的处理。
No.17 7月14日,荣昌生物维迪西妥单抗第2项适应症上市申请获国家药监局受理。预计该适应症为治疗HER2表达局部晚期或转移性尿路上皮癌。
No.18 7月14日,NMPA官网显示,阿斯利康PD-L1抑制剂度伐利尤单抗注射液新适应症上市申请获批,与依托泊苷联合铂类(卡铂或顺铂)化疗方案联合,用于广泛期小细胞肺癌的一线治疗。度伐利尤单抗是国内批准的首个PD-L1单抗,在2019年12月6日获批用于在接受铂类药物为基础的化疗同步放疗后未出现疾病进展的不可切除、III期非小细胞肺癌(NSCLC)患者的治疗。
No.19 7月13日,CDE官网显示华兰生物四价流感病毒裂解疫苗拟纳入优先审评,用于6个月至3岁以下人群预防相关型别的流感病毒引起的流行性感冒。接种本疫苗后,可刺激机体产生抗流感病毒的免疫力。
No.20 7月15日,贝达药业发出公告,宣布和 Agenus共同申报的巴替利单抗注射液(Balstilima,PD-1 抗体)和泽弗利单抗注射液(Zalifrelimab,CTLA-4 抗体)联用治疗晚期实体瘤的临床试验已获 NMPA 批准开展。
No.21 7月14日,迈博药业发出公告,称英夫利西单抗生物类似药(CMAB008)上市申请获NMPA批准上市,用于治疗成人溃疡性结肠炎、强直性脊柱炎、类风湿性关节炎、成人及6岁以上儿童克罗恩病、瘘管性克罗恩病、银屑病。这是国内首家获批上市的英夫利西单抗生物类似药。
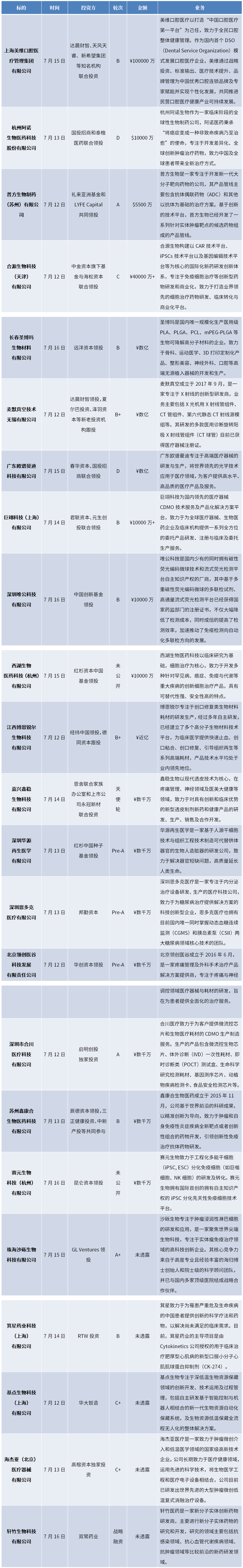
四、投融资
五、医药科技
No.1 7月15日,北京生命科学研究所/清华大学生物医学交叉研究院蒋辉实验室在《Cell Metabolism》发表了题为“Glycerol-3-phosphate biosynthesis regenerates cytosolic NAD+ to alleviate mitochondrial disease”的研究论文。该研究揭示了一条进化上保守的NAD+再生通路Glycerol-3-phosphate(Gro3P) biosynthesis, 并为呼吸链复合物I缺失导致的神经退行性疾病提供了治疗靶点。
文章配图(来源:Cell Metabolism)
No.2 7月15日,美国MD安德森癌症中心免疫学系孙少聪教授课题组题在《Blood》发表题为“DYRK1a mediates BAFF-induced noncanonical NF-κB activation to promote autoimmunity and B cell leukemogenesis”最新研究成果。该研究阐明了双特异性酪氨酸磷酸化调节激酶1a(DYRK1a)通过与肿瘤坏死因子受体作用因子3(TRAF3)相互作用并介导其磷酸化,从而促进非经典NF-κb信号通路的激活,进而影响这一疾病的发生发展,为该病的治疗提供了新的概念和药物靶点。
BAFF介导的非经典NF-κb信号通路(来源:Blood)
No.3 近日,维也纳医科大学的研究团队在《Science Translational Medicine》发表了题为“Down-regulation of A20 promotes immune escape of lung adenocarcinomas”的研究论文。该研究发现,肿瘤细胞内在的A20缺失显著增强了肺癌发生,并与CD8+ T细胞介导的免疫监测下降相关。在机制上该研究阐明了A20是调节TBK1-STAT1-PD-L1轴的主要免疫检查点,有望用于改善肺腺癌患者的免疫检查点治疗。
文章配图(来源:Science Translational Medicine)
No.4 德克萨斯心脏研究所 James Martin 团队在《Science Translational Medicine》发表了题为“Gene therapy knockdown of Hippo signaling induces cardiomyocyte renewal in pigs after myocardial infarction”的研究论文。该研究表明,通过基因疗法能够修复损伤的猪心肌细胞、减少疤痕大小并改善心脏功能。
No.5 近日,默沙东(MSD)宣布,其重磅抗PD-1疗法Keytruda,在治疗高风险早期三阴性乳腺癌(TNBC)的关键性3期临床试验中获得积极结果。在这项试验中,Keytruda与化疗联用作为新辅助疗法,并且在患者接受手术切除治疗后单药作为辅助疗法。这一治疗方案与新辅助化疗后辅助安慰剂相比,显著提高患者无事件生存期(EFS)。
No.6 7月13日,Hepion Pharmaceuticals公司宣布,在非酒精性脂肪性肝炎(NASH)患者中,其在研新型亲环素(cyclophilins)抑制剂CRV431的2a期AMBITION临床试验获得积极的顶线结果,达到试验的所有主要终点。